Изменение параметров иммунной системы в процессе т-клеточной вакцинации у больных ревматоидным артритом
© 2011 г. И.П. Иванова*, Г.В. Селедцова*, С.В. Мамаев***, Л.С. Литвинова**,
Ю.А. Лопатникова*, С.В. Сенников*, В.И. Селедцов**
* НИИ клинической иммунологии СО РАМН, г. Новосибирск, Россия;
** Балтийский федеральный университет им. И. Канта, г. Калининград, Россия;
*** ФМБА ФГУЗ Клиническая больница № 85, г. Москва, Россия
Поступила: 07.07.2011. Принята: 07.10.2011
Пациенты с ревматоидным артритом были пролечены с использованием вакцины, состоящей из аутологичных коллагенреактивных Т-клеток. Установлено, что после иммунотерапевтического курса лечения антиген-специфическая пролиферативная активность мононукле- арных клеток периферической крови пациентов значительно снижалась. Вакцинотерапия приводила также к достоверному снижению уровня IFNy и повышению уровня IL-4 в плазме крови пациентов. В соответствии с этим, у больных после курса лечения Т-клеточной вакциной отмечалось снижение числа IFNy-продуцирующих CD4+ и CD8 + клеток в 1,6 — 1,8 раза, а также параллельное увеличение числа IL-4-продуцирующих CD4+ лимфоцитов в 1,7 раза. Кроме того, в настоящем исследовании показано, что у больных ревматоидным артритом в сравнении со здоровыми лицами содержание CD8 + CD45RO + CD62L- эффекторных Т-клеток памяти и количество центральных CD4+CD45RO + CD62L+ и CD8 + CD45RO + CD62L+ Т-клеток памяти было увеличено в 5 — 7 раз. В процессе лечения у вакцинированных пациентов наблюдалось значительное снижение числа CD4+ и CD8+ центральных Т-клеток памяти, а также уменьшение количества эффекторных CD8+ Т-клеток памяти. Нами обнаружено также, что после вакцинации у больных достоверно увеличивалось количество регуляторных CD4+CD25 + FoxP3+ Т-клеток в периферической крови. Однако количество CD4+CD25- FoxP3+ Т-клеток существенно не менялось в процессе всего периода лечения. В результате клинического применения Т-клеточной вакцинации клиническое улучшение было достигнуто у 87% пациентов.
Ключевые слова: Т-клетки, вакцина, вматоидный артрит
Введение
Общепринято, что в основе патогенеза ревматоидного артрита (РА) лежит аутоиммунный процесс, опосредуемый Т-хелперами I типа. Специфическое распознавание Т-лимфоцитами антигенных молекул, экспрессирующихся на синовиальных суставных поверхностях, запускает цепь событий, приводящих к воспалению и разрушению суставов [1, 2].
Аутореактивные Т-клетки, распознающие собственные антигены, являются составной частью иммунной системы здорового организма. Это значит, что посттимические механизмы контролируют эти аутоагрессивные Т-клетки и обеспечивают защиту от них. Такая регуляция может включать периферическую клональную делецию, модуляцию антагонистами цитокинов, ингибицию взаимодействия идиотипов T-клеточных рецепторов (ТКР). Нарушенная регуляторная сеть приводит к нарушению подавления активированных аутоиммунных клеток и развитию аутоиммунного заболевания [2 — 4].
Является очевидным, что иммунотропное лечение РА должно быть направлено на инактивацию аутоиммунных Т- и В-лимфоцитов, усиление активности естественных и индуцированных регуляторных Т-клеток, подавление продукции провоспалительных медиаторов.
Т-клеточная вакцинация (ТКВ) — введение ослабленных аутореактивных Т-клеток — включает многие регуляторные механизмы иммунного ответа:
— ТКВ индуцирует антиклонотипические Т-клетки. Они регулируют патогенные Т-клетки через распознавание клонотипических детерминант (идиотипов), т.е. антиидиотипический ответ. В основном, это цитотоксические CD8 + Т-клетки, рестриктированные по молекулам МНС I класса. Меньшую долю составляют антиидиотипические CD4+ Т-клетки. Эти клетки не цитотоксичны для аутореактивных клеток, но ингибируют их пролиферацию, распознавая идиотипические детерминанты в комплексе с молекулами гистосовместимости II класса. Они могут принадлежать к разным типам Т-лимфоцитов: TH2 — продуцентам IL-4; TH3- продуцентам TGFp [4-7].
— ТКВ также затрагивает функцию естественных CD4 + CD25+ регуляторных Т-клеток (Treg). Имеются данные, предполагающие, что часть этих клеток обладает специфичностью к ТКР и исходно вовлечена в идиотипантиодиотипическую иммунорегуляцию. Это означает, что Т-клеточная вакцинация может создавать благоприятные условия для экспансии CD4+CD25+ T reg, специфичных к вакцинальным ТКР [8].
— ТКВ воздействует на антиэрготипическую регуляцию Т-клеточных реакций, которая не связана с распознаванием идиотипических детерминанат. Независимо от своей антигенной специфичности, антиэрготипические Т-клетки реагируют только на активированные, а не покоящиеся аутореактивные Т-клетки [4, 9].
— ТКВ индуцирует не только Т-, но и В- клеточные реакции, а именно, образование антиидиотипических антител, которые связываются и ингибируют аутореактивные Т-клеточные клоны. Они относятся к IgG, распознают ТКР-детерминанты вне зависимости от молекул главного комплекса гистосовестимости. Механизм действия таких антител может быть связан с экранированием и функциональной блокадой ТКР [10].
Таким образом, имеющиеся экспериментальные и клинические данные дают основание полагать, что ТКВ может стать эффективным методом лечения аутоиммунных заболеваний, имеющим большой потенциал для своего дальнейшего развития [11, 12].
Целью настоящей работы было исследование иммунологических и клинических аспектов применения Т-клеточной вакцинации у больных РА.
Материалы и методы
Технология получения Т-клеточной вакцины
Разработанная нами технология получения Т-клеточной вакцины состоит из двух последовательных этапов. Первый этап включает в себя специфическую селекцию клеток, тогда как второй — их наращивание в необходимом количестве [13, 14]. На первом этапе выделенные из периферической крови мононуклеарные клетки (МНК) пациентов культивировали в концентрации 2×106 мл в среде RPMI 1640, содержащей 10% инактивированной аутологичной плазмы, 5 мМ HEPES, 2 мМ L-глутамина, 5×10-5 М меркаптоэтанола (все реагенты компании «Sigma», США) в присутствии синовиальных (1 мкг/мл) и хрящевых (1 мкг/мл) антигенов в течение 5— 7 дней во влажной атмосфере с 5% СО2. Хрящевые и синовиальные белковые антигены получены из суставных тканей свиньи. Антиген хрящевой ткани выделяли методом, описанным Strom S.C. [15]. Синовиальный белковый антиген получали путем центрифугирования синовиальной жидкости. На втором этапе антигенспецифические клетки наращивали посредством их стимуляции фитогемагглютинином (ФГА, 5 мкг/мл, «Sigma») и рекомбинантным IL-2 (100 ед/мл, «Биотех», Санкт- Петербург) в течение 5 дней. По завершению культивирования клетки инактивировали, далее криоконсервировали стандартным путем в плазме с 10% диметилсульфоксида («Sigma») и хранили в жидком азоте до момента использования. Общее количество полученных от одного больного клеток вакцины варьировало в пределах 18—27×107.
Пролиферативный ответ полученных таким образом вакцинальных клеток на хрящевые и синовиальные антигены превышал контрольные значения 1,8 — 2,0 раза. В процессе культивирования число IFNy-продуцирующих CD4+ и CD8+ Т-клеток увеличивалось от 3 до 10 раз, содержание CD3 + СD45RO+ Т-клеток памяти увеличивалось в 2 раза, а содержание CD3 + СD45RА+ — в 1,3 раза [16].
Оценка пролиферативного ответа МНК
Для оценки антиген-индуцированного пролиферативного ответа МНК культивировали в 96-луночном планшете в концентрации 2×105 в полной среде в присутствии хрящевых (1 мкг/мл) и синовиальных (1 мкг/мл) антигенов либо без них в течение 5 дней во влажной атмосфере с 5% СО2. Клеточная пролиферация учитывалась стандарным методом по включению [3Н] тимидина.
Определение цитокинов в плазме крови и культуральных жидкостях
Количественное содержание цитокинов — IFNy и IL-4 в образцах плазмы крови и супернатантах 72-часовых культур МНК оценивали иммуноферментным методом с использованием коммерческих тест-систем компании «Вектор-Бест» (п. Кольцово, Новосибирская область).
Оценка содержания IFNy- и IL-4 — продуцирующих лимфоцитов
Количество IFNy- и IL-4- продуцирующих лимфоцитов оценивали с помощью метода определения внутриклеточных цитокинов после 4 ч культивирования МНК периферической крови в присутствии форболового эфира, иономицина и брефелдина А. По окончании периода культивации клетки обрабатывали моноклональными антителами к поверхностным маркерам (CD4 и CD8) и после фиксации и пермеабилизации инкубировали в присутствии моноклональных антител (МА) к IFNy и IL-4 (все реактивы «Becton Dickinson», США). После отмывки клетки анализировали на проточном цитометре.
Определение содержания Т-клеток памяти
Относительное содержание клеток памяти определяли методом 3-цветной проточной цитофлюориметриии с помощью меченных фикоэритрином (РЕ) МА к CD4 и CD8 («Сорбент», Москва), конъюгированных с флюоресцеинизотиоцианатом (FITC) МА к CD45RO («eBioscience», США), меченных аллофикоцианином (APC) анти-CD62L МА («eBioscience», США). По наличию или отсутствию на клеточной поверхности соответствующих молекул определяли следующие клеточные популяции: наивные клетки — (CD45RO"CD62L+), центральные клетки памяти — (CD45RO+CD62L+), эффекторные клетки памяти — (CD45RO+CD62L«). В тексте указан процент каждой популяции от общего числа лимфоцитов.
Определение содержания регуляторных Т-клеток
Поверхностные маркеры регуляторных (CD4+CD25+FoxP3 + ) клеток определяли с помощью МА к CD4, меченных АРС; МА к IL-2 рецептору (CD25), конъюгированных с FITC. Экспрессию FoxP3 оценивали с использованием МА, меченных РЕ (все реактивы «Becton Dickinson», США). Процент позитивных от общего числа лимфоцитов клеток определяли на проточном цитометре «FACS Calibur».
Клинические исследования
Клинические и экспериментальные исследования проводили в соответствии с протоколом, утвержденным Ученым советом и Этическим комитетом Института клинической иммунологии СО РАМН. От каждого пациента, участвующего в исследовании, было получено информированное согласие. Иммунотерапевтическое лечение было проведено 42 больным РА (37 женщин, 5 мужчин) в возрасте от 28 до 58 лет с давностью заболевания не менее 2 лет. Клинические испытания проводили на базе ФМБА ФГУЗ Клинической больницы № 85, г. Москва. Все пациенты получали базисную терапию метотрексатом в дозе не более 10 мг в неделю. Дополнительно схема лечения Т-клеточной вакциной включала в себя 4 еженедельных подкожных вакцинации (индуцирующий курс) и последующие вакцинации с интервалом в 1 месяц. Вакцинальная доза варьировала в пределах 2,0 — 4,0×107 клеток. Для оценки эффективности лечения Т-клеточной вакциной использовали критерии Европейской антиревматической лиги (EULAR), основанные на динамике DAS 28 [19]. Кроме того, анализировали отдельные показатели активности РА: интенсивность боли, длительность утренней скованности, число болезненных и число припухших суставов, СОЭ, параметры качества жизни (HAQ).
Для иммунологического исследования составили контрольную группу из 10 здоровых доноров, сопоставимых по возрасту.
Статистическую обработку результатов проводили с использованием критерия U Вилкоксона-Манна-Уитни, парного критерия Вилкоксона.
Результаты
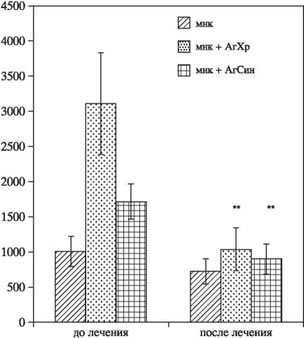
Рис. 1. Пролиферативный ответ МНК периферической крови больных РА (n = 12) на специфические антигены (хрящевой и синовиальный) до и через 1 год после начала лечения.
** Р < 0,01 — статистическая значимость различий, критерий U
Пролиферативный ответ и продукция про- и противовоспалительных цитокинов МНК периферической крови больных РА
В процессе лечения Т-клеточной вакциной пролиферативный ответ МНК больных РА в ответ на хрящевые и синовиальные антигены достоверно снижался (рис. 1). Это может свидетельствовать об уменьшении количества аутоантиген-реактивных клеток в организме пациента.
Вакцинотерапия приводила также к значительному и стойкому снижению уровня IFNy и увеличению уровня IL-4 в плазме крови через 6 месяцев после начала лечения (рис. 2). МНК вакцинированных пациентов в присутствии антигенов суставных тканей отличались пониженной способностью к продукции IFNy и повышенной способностью к продукции IL-4 по сравнению с исходными (до начала терапии) значениями (данные не представлены). В соответствии с этим, у больных РА уже после индуцирующего курса лечения Т-клеточной вакциной отмечалось достоверное снижение IFNy- продуцирующих CD4+ и CD8+ клеток в 1,6 — 1,8 раза, а также параллельное увеличение числа IL-4- продуцирующих CD4+ лимфоцитов в 1,7 раза (рис. 3).
Исследование относительного содержания Т-клеток памяти
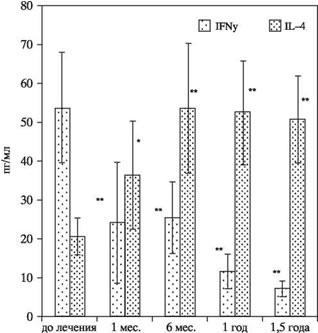
Рис. 2. Содержание IFNy и IL-4 в плазме крови больных РА (n = 12) в динамике лечения.
* Р < 0,05; ** Р < 0,01 — статистическая значимость различий в сравнении с исходным уровнем, критерий U.
В результате проведенного исследования нами обнаружено, что у как у здоровых лиц, так и у больных РА количество «наивных» CD4+CD45RO-CD62L+ и CD8+CD45RO’ CD62L+ существенно не различалось (таб. 1). В то же время, у больных РА содержание CD8+CD45Ro+Cd62L" эффекторных клеток памяти было увеличено в 5 раз, а количество центральных клеток памяти CD45RO+CD62L+ было увеличено как среди CD4+, так и среди CD8+ Т-клеток. Наши данные указывают, что при РА может иметь место ускоренная диффе- ренцировка «наивных» клеток в центральные CD4+ и CD8+ Т-клетки и цитотоксические эффекторные CD8+ Т-клетки, которая отражает антигенспецифическую экспансию Т-клеток в ответ на повторные, системные воздействия антигена [17, 18].
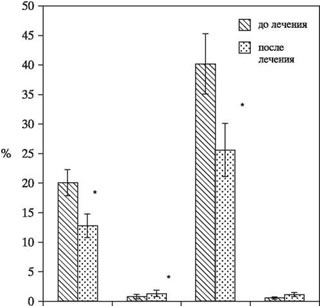
Рис. 3. Содержание IFNy и IL-4-продуцирующих лимфоцитов (CD4 и CD8) в периферической крови больных РА (n = 7) до и после индуцирующего курса лечения.
* P < 0,05 — статистическая значимость различий по сравнению с исходным уровнем, парный критерий Вилкоксона.
В процессе лечения у вакцинированных пациентов уже через 1 мес. наблюдалось достоверное и значительное (в 5 — 6 раз) снижение числа CD4+ и CD8 + центральных клеток памяти, а также уменьшение в 2 раза количества эффекторных CD8+ клеток памяти. Полученный эффект поддерживался в течение 9 мес. от начала вакцинации, после чего количественные характеристики клеток памяти возвращались к величинам, близким исходным.
Исследование относительного содержания регуляторных Т-клеток
Представленные на рис. 4 данные показывают, что, по сравнению с донорами, в периферической крови больных РА отмечается незначительное снижение количества регуляторных «наивных» CD4+CD25+FoxP3 + Т-клеток, которое уже через 1 мес. после начала вакцинации достоверно увеличивается (практически в 6 раз). Этот эффект прослеживается в течение 6 мес. от начала лечения, а затем постепенно уменьшается. Что касается популяции индуцированных CD4+CD25- FoxP3+ Т-клеток, то их число существенно не меняется в процессе всего периода лечения.
Результаты клинических испытаний
Таблица 1. Содержание субпопуляций Т-клеток у больных РА в процессе лечения Т-клеточной вакциной (M ± m)
|
|
Доноры n = 10 |
Больные до лечения n = 42 |
Больные после лечения 1 мес n = 10 |
Больные после лечения 6 мес n = 15 |
Больные после лечения 9 мес n = 10 |
Больные после лечения 1 г n = 10 |
|
CD4+CD45RO+ CD62L+ |
1,11±0,48 |
4,23±0,76* |
0,75±0,39* |
2,07±0,68 |
0,12±0,04* |
3,1±0,96 |
|
CD4+CD45RO+ CD62L- |
9,28±4,16 |
7,67±1,08 |
6,72±3,8 |
7,35±1,49 |
2,42±0,63* |
6,02±1,16 |
|
CD4+CD45RO-CD62L+ |
10,18±3,86 |
6,66±0,83 |
6,6±1,75 |
4,49±0,69 |
7,18±3,14 |
9,25±3,3 |
|
CD4+CD45RO-CD62L- |
24,11±5,7 |
23,52±2,12 |
30,44±4,6 |
29,17±3,82 |
41,2±7,63 |
27,85±6,6 |
|
CD8 + CD45RO+ CD62L+ |
0,1±0,03 |
0,74±0,16* |
0,13±0,004* |
0,52±0,23 |
0,12±0,07* |
0,96±0,3 |
|
CD8 + CD45RO+ CD62L- |
0,31±0,07 |
1,59±0,28* |
0,7±0,2* |
1,21±0,3 |
0,84±0,29* |
1,91±0,59 |
|
CD8 + CD45RO-CD62L+ |
3,93±1,29 |
3,06±0,34 |
3,04±0,7 |
2,52±0,43 |
2,68±1,57 |
3,48±0,77 |
|
CD8 + CD45RO-CD62L- |
11,47±1,77 |
14,18±1,03 |
15,77±2,11 |
14,99±1,32 |
16,04±2,18 |
10,91±1,4 |
* P < 0,05 — статистическая значимость различий показателей при сравнении группы доноров и больных до начала лечения, а также в группах вакцинированных больных по сравнению с исходным уровнем (критерий U).
Результаты оценки клинической эффективности Т-клеточной вакцинации у пациентов с РА свидетельствуют о хорошем/умеренном клиническом эффекте (по критериям EULAR) применяемого курса лечения. Это подтверждается достоверным и стойким снижением индекса DAS28, снижением интенсивности болевого синдрома, числа болезненных и числа припухших суставов, продолжительности утренней скованности и утомляемости начиная с 3 мес. после начала терапии (таб. 2).
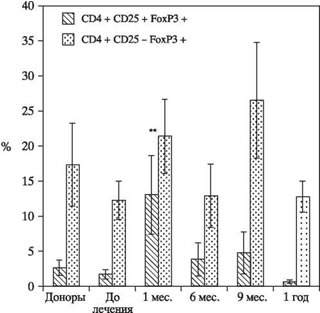
Рис. 4. Количественное содержание регуляторных Т-клеток у больных РА в процессе лечения Т-клеточной вакциной.
** P < 0,01 — статистическая значимость различий показателей по сравнению с исходным уровнем, критерий U.
При более подробном анализе результатов установлено, что на фоне лечения хороший и умеренный эффект был достигнут к 6 мес. у 91,5% пациентов и только у 9,5% больных улучшения не было зарегистрировано. При этом у 28,5% развилась клиническая ремиссия (DAS < 2,6 ед.). Эффект лечения был стойким, и сохранялся в течение 2 лет от начала терапии. К 24 мес. наблюдения хорошие и умеренные результаты были зарегистрированы у 87% больных, низкая степень активности отмечена у 63,6%, а состояние клинической ремиссии достигнуто у 40,9% пациентов. Переносимость вакцинации, в целом, была удовлетворительной, только в одном случае наблюдалась местная реакция в виде покраснения кожи и в двух случаях отмечалось повышение температуры тела. Все побочные эффекты не требовали прекращения лечения и купировались самостоятельно.
Обсуждение
Традиционное лечение РА основано на длительной неспецифической иммуносупрессирующей терапии, которая снижает иммунитет в целом и имеет высокий риск развития серьезных побочных эффектов. Имеется очевидная необходимость поиска новых подходов к лечению РА и других аутоиммунных заболеваний, нацеленных на избирательную инактивацию патогенных, аутореактивных лимфоцитов. Один из таких подходов базируется на вакцинации пациента аутоиммунными лимфоцитами, так как хорошо известно, что к антигенным рецепторам лимфоцитов, сформированным в постнатальный период, нет врожденной иммунологической толерантности и межлимфоцитарные идиотип- антиидиотипические взаимодействия играют важную роль в регуляции функционирования иммунной системы.
Таблица 2. Динамика суставного синдрома и лабораторных показателей в процессе Т-клеточной вакцинации (M ± m)
| Показатель | Время исследования | |||||
| До лечения (n = 42) | 3 мес. (n = 42) | 6 мес. (n = 42) | 12 мес. (n = 42) | 18 мес. (n = 32) | 24 мес. (n = 22) | |
| СОЭ (мм/ч) | 38,4±2,2 | 31,12±1,94** | 22,81±1,26** | 21,75±1,6** | 1 20,19±1,74** | 21,14±2,12** |
| Гемоглобин (г/л) | 107,8±1,45 | 113,7±1,25** | 120,8±1,01** | 125,2±0,98** | 126,4±1,17** | 126,4±1,88** |
| Число болезненных суставов | 11,90±0,63 | 7,26±0,56** | 2,57±0,47** | 2,09±0,43** | 2,12±0,53** | 2,41±0,76** |
| Число припухших суставов | 6,97±0,56 | 4,19±0,55** | 1,33±0,4** | 0,83±0,33** | 1,01±0,40** | 1,22±0,52** |
| HAQ | 2,32±0,06 | 1,78±0,11** | 1,26±0,12** | 0,87±0,12** | 0,91±0,14** | 1,11±0,14** |
| Утренняя скованность (мин) | 78,10±5,04 | 47,76±5,16** | 20,0±4,29** | 12,38±3,52** | 12,38±4,4** | 14,09±5,53** |
| Боль ,VAS(мм) | 60,12±2,65 | 39,40±2,94** | 16,9±2,79** | 11,60±2,09** | 10,78±2,46** | 11,14±3,14** |
| Утомляемость, VAS (мм) | 54,29±2,46 | 34,83±3,07** | 14,81±2,81** | 9,92±2,37** | 10,06±2,55** | 10,59±3,25** |
| DAS 28 | 5,92±0,13 | 4,93±0,16** | 3,34±0,18** | 2,99±0,17** | 2,96±0,21** | 3,12±0,27** |
Р < 0,001 — статистическая значимость различий в группах до и после лечения (критерий U).
Очевидное преимущество ТКВ перед другими методами лечения заключается не только в ее избирательной направленности на инактивацию именно тех лимфоцитов, которые ответственны за развитие аутоиммунного процесса. Особенно важным представляется то, что механизм влияния ТКВ включает в себя целый ряд компонентов: стимуляцию анти-идиотипических иммунных реакций, индукцию и стимуляцию функциональной активности T reg, индукцию синтеза анти-идиотипических антител и др. Следует признать, что данных по клиническому применению метода ТКВ пока явно недостаточно. Ранее, в большинстве исследований для иммунизации использовались клонированные Т-лимфоциты. Однако, наработка Т-клеточных клонов — процедура дорогая, длительная и далеко не всегда заканчивающаяся успехом. Кроме того, инактивация одного или нескольких аутоиммунных клонов может не оказать существенного влияния на развитие заболевания, которое может быть обусловлено поликлональным иммунным ответом, направленным против множества антигенных детерминант, где значимость одного отдельного клона в аутоиммунном процессе может оказаться несущественной. Все это ограничивает возможности эффективного применения клонированных Т-клеток в лечении как РА, так и других аутоиммунных заболеваний.
Разработанный в нашей лаборатории метод позволяет за относительно короткое время получить достаточное количество аутоантиген- реактивных Т-клеток. При этом состав вакцины определяется исходной индивидуальной реактивностью Т-клеток и представлен наиболее аутоагрессивными клетками, которые получали селективные ростовые преимущества, связанные с присутствием в культуре антигенов суставных тканей.
Одной из основных целей проведенного нами пилотного клинического исследования являлась оценка иммунологической и клинической эффективности предлагаемого способа лечения. На иммунологическую эффективность ТКВ указывает значительное снижение пролиферативной активности МНК больных в ответ на воздействие тканевых суставных антигенов, которая может отражать снижение числа антиген-реактивных клеток в организме. Важное значение имеют также изменения в концентрации IFNy и IL-4, выявленные в плазме крови и супернатантах МНК вакцинированных пациентов. Снижение первого и повышение второго указывает на функциональную перестройку иммунной системы и включение неспецифических иммунных механизмов в торможение иммунопатологического процесса. Считается, что при РА, продуцируемый Т-хелперами 1 типа, IFNy играет ключевую роль в вовлечении макрофагов и других иммунокомпетентных клеток в патологическое воспаление, тогда как, продуцируемый Т-хелперами 2 типа, IL-4 способен снижать этот, опосредуемый IFNy, эффект и, таким образом, оказывать противовоспалительное действие.
Снижение числа центральных и, в особенности, эффекторных CD8 + клеток памяти в результате иммунотерапии также является благоприятным признаком для развития заболевания, так как продуцирующие IFNy, TNFa и перфорин CD8+ Т-клетки участвуют в активации макрофагов и поддержании хронического воспаления и деструкции тканей сустава.
С другой стороны, ослабление аутоиммунных реакций может быть, по-видимому, достигнуто за счёт зарегистрированного в нашем исследовании увеличения количества или усиления функциональной активности CD4+CD25+FoxP3+ регуляторных Т-клеток, которые способны оказывать выраженное негативное влияние как на генерацию клеток иммунной памяти, так и на функции эффек- торных клеток [20].
Полученные результаты также предполагают наличие значимой клинической эффективности применения Т-клеточной вакцинации, так как хороший и умеренный эффект лечения был достигнут у 87% больных.
Таким образом, ТКВ открывает новые возможности в лечении РА и других аутоиммунных заболеваний. Она хорошо переносится, не имеет значительных побочных эффектов, ограничивающих её клиническое применение, позволяет индуцировать в иммунной системе долговременные изменения, препятствующие прогрессии заболевания. Очевидно, что развитие этой технологии и получение новых данных, связанных с её применением, чрезвычайно востребовано современной медициной.
Список литературы
1. Stamenkovic I., Stegagno M., Wright K.A., Krane S.M., Amento E.P. et al. Clonal dominance among T-lymphocyte infiltrates in arthritis. Proc. Natl. Acad. Sci. USA 1998, 85, 1179-1183.
2. VanderBorght A., Geusens P., Raus J., Stinissen P. The autoimmune pathogenesis of rheumatoid arthritis: role of autoreactive T cells and new immunotherapies. Semin. Arthritis Rheum, 2001, 31, 160-175.
3. Fekete A., Soos L., SzekaneczZ., Szabo Z., SzodorayP. et al. Disturbances in B- and T-cell homeostasis in rheumatoid arthritis: suggested relationship with antigen-driven immune responses. J. Autoimmun. 2007, 29(2-3), 154-163.
4. Correale J., Farez M., Gilmore W. Vaccines for multiple sclerosis. CNS Drugs 2008, 22(3), 175198.
5. Honda A., Ametani A., Matsumoto T., Iwaya A., Kano H.et al.Vaccinationwith an immunodominant peptide of bovine type II collagen induces an anti-TCR response, and modulates the onset and severity of collagen-induced arthritis. Int. Immunol. 2004, 16, 737-745.
6. Moreland L.W., Heck L.W., Koopman W.J., SawayP.A., Adamson T.C. et al. Vp 17 T cell receptor peptide vaccination in rheumatoid arthritis: results of phase 1 dose escalation study. J. Rheumatol. 1996, 23, 1353-1362.
7. Zang Y.C.Q., Hong J., Tejada-Simon M.V., Li S., Rivera V.M. et al. Th 2 immune regulation induced by T cell vaccination in patients with multiple sclerosis. Eur. J.Immunol. 2000, 30, 908-913.
8. Vandenbark A.A. TCR peptide vaccination in multiple sclerosis: Boosting a deficient regulatory network that may involve TCRspecific CD4+CD25+ Treg cells. Curr. Drug Targets Inflamm. Allergy 2005, 4, 85-94.
9. Hellings N., Raus J., Stinissen P. T cell vaccination in multiple sclerosis: update on clinical application and mode of action. Autoimm. Rev. 2004, 3, 267275.
10. Hong J., Zang Y.C.Q., Tejada-Simon M.V., Li S., Rivera V.M., Killian J. et al. Reactivity and regulatory properties of human anti-idiotypic antibodies induced by T cell vaccination. J. Immunol. 2000, 165, 6858-6864.
11. Селедцов Д.В., Селедцов В.И., Иванова И.П., Литвинова Л.С. Антиген-специфическая иммунотерапия рассеянного склероза. Цитокины и воспаление 2010, 9(1), 3-12.
12. Vandenbark A.A., Morgan E., Bartholomew R., Bourdette D., WhithamR. et al. TCR peptide therapy in human autoimmune diseases. Neurochem. Res. 2001, 26, 713-730.
13. Селедцов В.И., Иванова И.П., Самарин Д.М., Козлов В.А. Способ получения поликлональной Т-клеточной вакцины для лечения иммунологических расстройств. РФ, Патент на изобретение № 2277422, 10 июня 2006 г.
14. Иванова И.П., Селедцов В.И., Банул Н.В., Самарин Д.М., Селедцова Г.В. и др. Получение Т-клеточной вакцины и ее применение для лечения рассеянного склероза. Медицинская Иммунология 2005, 7(1), 27-32.
15. Strom S.C., Michalopoulos G. Collagen as a substrate for cell growth and differentiation. Methods Enzymol. 1982, 82(A), 554-555.
16. Иванова И.П., Селедцов В.И., СеледцовД.В., Самарин Д.М., Селедцова Г.В. и др. Характеристика иммуногенных свойств поликлональной Т-клеточной вакцины, предназначенной для лечения ревматоидного артрита. Клеточные технологии в биологии и медицине 2007, 4, 221-226.
17. Nanki T., Lipsky P.E. Cytokine, activation marker, and chemokine receptor expression by individual CD4+ memory T cells in rheumatoid arthritis synovium. Arthritis Res. 2000, 2(5), 415-423.
18. Селедцов В.И., Литвинова Л.С., Гончаров А.Г., Щуплецова В.В., Селедцов Д.В. и др. Клеточные механизмы генерации иммунологической памяти. Цитокины и воспаление 2010, 9(4), 9-15.
19. Fransen J., Stucki G., van Riel P.L.C. Rheumatoid arthritis measures. Arthr. & Rheum. 2003, 49, 214-224.
20. Corthay A. How do regulatory T cell work? Scand. J. Immunol. 2009, 70(4), 326-336.
CHANGES OF IMMUNE PARAMETRS DURING T-CELLS
VACCINATION IN PATIENTS WITH RHEUMATOID ARTHRIRIS
I.P. Ivanova*, G.V. Seledtsova*, S.V. Mamaev***, L.S. Litvinova**, J.A.
Lopatnikova*, S.V. Sennikov*, V.I. Seledtsov**
Research Institute of Clinical Immunology, Siberian Division of Russian Academy of Medical
Sciences, Novosibirsk, Russia;
**
Baltic Federal University of Immanuel Kant, Kaliningrad, Russia;
Clinical Hospital № 85, Moscow, Russia
Rheumatoid arthritis patients were treated with an vaccine consisted of autological collagen- reactive T-cells. It was established, that antigen-specific, proliferative activity of the patients’ peripheral blood mononuclear cells was a significantly decreased after immunotherapy course. A significant decrease in IFNy level and an increase in IL-4 level were noted in the plasma of vaccine- treated patients. In accordance with this, after course of T-cells vaccination the number of IFNy- producing CD4+ and CD8+ cells was decreased (by 1,6 — 1,8 fold) in patients, whereas the number of IL-4-producing CD4+ lymphocytes was increased by 1,7 fold. In addition, the present study showed that effector memory CD8+CD45RO+CD62L- T-cells and central memory CD4+CD45RO+CD62L+ and CD8+CD45RO+CD62L+ T-cells were significantly increased (by 5 — 7 fold) in rheumatoid arthritis patients as compared with levels in healthy individuals. During the treatment the peripheral blood central memory CD4+ and CD8+ T-cells, as well the effector memory CD8+ T-cells levels significantly decreased in vaccinated patients. We revealed that after vaccinotherapy regulatory CD4+CD25+FoxP3+ T-cell levels significantly increased in the patients’ peripheral blood. However, amount of CD4+CD25-FoxP3+ Т-cells did not change during all treatment courses. As the result of the T-cell vaccine clinical application it has been established that clinical improvement was achieved in 87% patients.
